 退出登录
退出登录【热点评论】药品检验报告在假劣药认定中的作用
以下文章来源于医药法那些事,作者姚嘉 律师
药品检验报告在假劣药认定中的作用可以概括为:认定假劣药并非一定要有检验报告,检验不合格也不一定都认定为假劣药。
《药品管理法(2019修订)》(以下简称2019药法)第一百二十一条规定:对假药、劣药的处罚决定,应当依法载明药品检验机构的质量检验结论。
该条文表述删去了《药品管理法(2015修订)》(以下简称2015药法)第七十七条中的“但是”,增加了“依法”二字。2019药法实施后,实践中对于假药、劣药的认定是否全部需经检验曾存有争议。
此后,国家药监局综合司在给贵州省药品监督管理局《关于假药劣药认定有关问题的复函》(药监综法函〔2020〕431号)(以下简称复函)中明确,对假药、劣药的处罚决定,有的无需载明药品检验机构的质量检验结论。
由于复函法律效力较低,前不久公开的《药品管理法实施条例(修订草案征求意见稿)》(以下简称条例征求意见稿)第一百七十条对此问题也进行了规定。
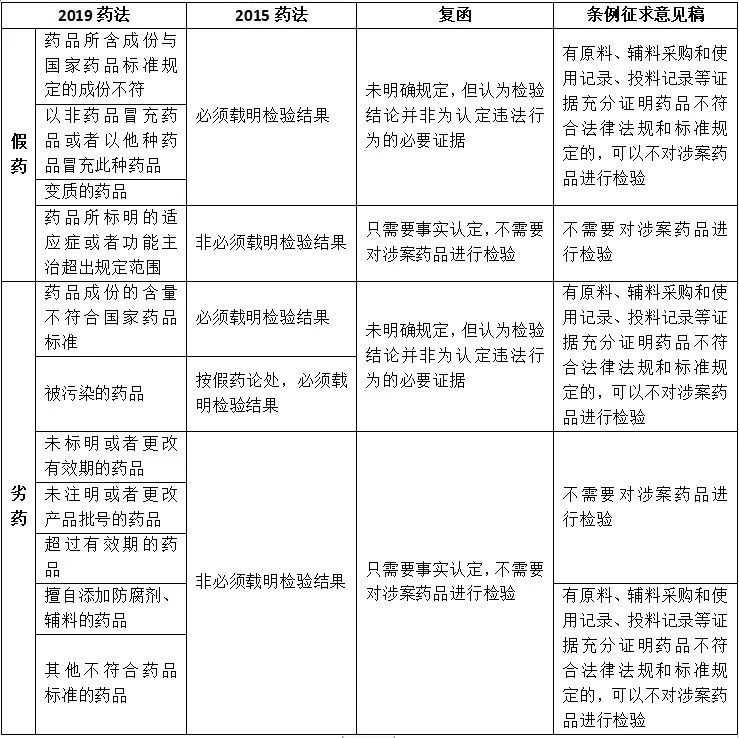
比较而言,条例征求意见稿第一百七十条的规定更具合理性。归根结底,认定假劣药需有充分的证据,检验报告只是证据的其中一种,只要其他证据足够充分,检验报告并非必须。
既然检验报告是证据的一种,那么,实务中就存在检验结论为不合格,但并未被作为认定为假劣药依据的情形。常见情况是复验结论推翻了原检验结论。此外,笔者还曾遇到一些特殊情况。
案例1
A药业公司为氟康唑胶囊生产企业,该药品执行标准为2015版《中华人民共和国药典》,药典中对氟康唑胶囊性状描述为:本品的内容物为白色或类白色粉末。该公司生产的氟康唑胶囊经某市药品检验所检验,性状检验结果为白色颗粒,结论为“不符合规定”。
然而该药品获批的《氟康唑胶囊生产工艺规程》中生产工艺为湿法制粒。此外,参照国家药典委员会《关于国家标准有关内容执行问题的函》(国药典化发〔2007〕8号)意见:由于企业采用不同灌装设备,胶囊剂内容物外观形状与标准中【性状】项下描述不同(如出现柱状或块状等)时,应判定符合规定。
因此该不合格检验报告不宜作为认定劣药的依据。(目前国家药典委员会已将氟康唑胶囊性状修订为:本品的内容物为白色或类白色粉末或颗粒。)
案例2
B药业公司生产的硫酸氨基葡萄糖胶囊经抽检结论为不符合标准,不合格项目为“其他未知杂质总含量”超标。
后经进一步调查发现,硫酸氨基葡萄糖胶囊所用原料药是以盐酸氨基葡萄糖溶于水,用树脂将氯离子吸附后,加入硫酸生成硫酸氨基葡萄糖。
氯化物是原料中带入的已知杂质而非未知杂质。而检验机构由于采用的检验方法原因,将氯离子峰当做未知杂质进行计算,从而导致“其他未知杂质总含量”超标。
该不合格检验报告也不宜作为认定劣药的依据。
案例3
C药业公司生产的某药品的标准要求pH值为6.8—7.6,经检验pH值为7.64,检验结论为不符合标准要求。
由于该药品标准中的pH值保留小数点后一位,根据《中华人民共和国药典》《中国药品检验标准操作规范》修约规则和GB/T 8170-2008《数值修约规则与极限数值的表示和判定》,在药品检验中7.64应修约至7.6报告,检验结论实际应为合格。
该不合格检验报告不宜作为认定劣药的依据。
总之,是否将检验结论作为认定为假劣药依据,应具体情况具体判断。
 蜀ICP备20020612号
蜀ICP备20020612号